Η φύση του χρωμίου
Το χρώμιο, σύμβολο στοιχείου Cr, ατομικός αριθμός 24, σχετική ατομική μάζα 51.996, ανήκει στο μεταλλικό στοιχείο μεταπτώσεως της ομάδας VIB του περιοδικού πίνακα των χημικών στοιχείων. Το μέταλλο χρώμιο είναι κυβικός κρύσταλλος με κέντρο το σώμα, ασημί-λευκό, πυκνότητα 7,1 g/cm³, σημείο τήξης 1860℃, σημείο βρασμού 2680℃, ειδική θερμοχωρητικότητα στους 25℃ 23,35J/(mol·K), θερμότητα εξάτμισης 1kJ/342. mol, θερμική αγωγιμότητα 91,3 W/(m·K) (0-100°C), ειδική αντίσταση (20°C) 13,2uΩ·cm, με καλές μηχανικές ιδιότητες.
Υπάρχουν πέντε σθένη του χρωμίου: +2, +3, +4, +5 και +6. Υπό τις συνθήκες ενδογενούς δράσης, το χρώμιο είναι γενικά +3 σθένους. Οι ενώσεις με +τρισθενές χρώμιο είναι οι πιο σταθερές. +Οι ενώσεις εξασθενούς χρωμίου, συμπεριλαμβανομένων των αλάτων του χρωμίου, έχουν ισχυρές οξειδωτικές ιδιότητες. Οι ιοντικές ακτίνες των Cr3+, AI3+ και Fe3+ είναι παρόμοιες, επομένως μπορούν να έχουν ένα ευρύ φάσμα ομοιοτήτων. Επιπλέον, τα στοιχεία που μπορούν να αντικατασταθούν με χρώμιο είναι το μαγγάνιο, το μαγνήσιο, το νικέλιο, το κοβάλτιο, ο ψευδάργυρος κ.λπ., επομένως το χρώμιο είναι ευρέως διανεμημένο σε ορυκτά πυριτικού σιδήρου μαγνησίου και βοηθητικά ορυκτά.
Εφαρμογή
Το χρώμιο είναι ένα από τα πιο ευρέως χρησιμοποιούμενα μέταλλα στη σύγχρονη βιομηχανία. Χρησιμοποιείται κυρίως στην παραγωγή ανοξείδωτου χάλυβα και διαφόρων κραματοποιημένων χάλυβων σε μορφή σιδηροκράματος (όπως το σιδηρόχρωμο). Το χρώμιο έχει τα χαρακτηριστικά του σκληρού, ανθεκτικό στη φθορά, ανθεκτικό στη θερμότητα και ανθεκτικό στη διάβρωση. Το μετάλλευμα χρωμίου χρησιμοποιείται ευρέως στη μεταλλουργία, τα πυρίμαχα υλικά, τη χημική βιομηχανία και τις βιομηχανίες χυτηρίου.
Στη μεταλλουργική βιομηχανία, το μετάλλευμα χρωμίου χρησιμοποιείται κυρίως για την τήξη σιδηροχρωμίου και μεταλλικού χρωμίου. Το χρώμιο χρησιμοποιείται ως πρόσθετο χάλυβα για την παραγωγή μιας ποικιλίας ειδικών χάλυβων υψηλής αντοχής, ανθεκτικών στη διάβρωση, ανθεκτικών στη φθορά, υψηλής θερμοκρασίας και οξείδωσης, όπως ανοξείδωτος χάλυβας, ανθεκτικός στα οξέα χάλυβας, χάλυβας ανθεκτικός στη θερμότητα, Χάλυβας ρουλεμάν, χάλυβας ελατηρίου, χάλυβας εργαλείων κ.λπ. Το χρώμιο μπορεί να βελτιώσει τις μηχανικές ιδιότητες και την αντοχή στη φθορά του χάλυβα. Το μεταλλικό χρώμιο χρησιμοποιείται κυρίως για την τήξη ειδικών κραμάτων με κοβάλτιο, νικέλιο, βολφράμιο και άλλα στοιχεία. Η επιχρωμίωση και η επιχρωμίωση μπορούν να κάνουν τον χάλυβα, τον χαλκό, το αλουμίνιο και άλλα μέταλλα να σχηματίσουν μια ανθεκτική στη διάβρωση επιφάνεια, η οποία είναι φωτεινή και όμορφη.
Στη βιομηχανία πυρίμαχων υλικών, το μετάλλευμα χρωμίου είναι ένα σημαντικό πυρίμαχο υλικό που χρησιμοποιείται για την κατασκευή τούβλων χρωμίου, τούβλων χρωμίου μαγνησίας, προηγμένων πυρίμαχων υλικών και άλλων ειδικών πυρίμαχων υλικών (χρωμιωμένο σκυρόδεμα). Τα πυρίμαχα με βάση το χρώμιο περιλαμβάνουν κυρίως τούβλα με μετάλλευμα χρωμίου και μαγνησία, πυροσυσσωματωμένο κλίνκερ μαγνησίας-χρωμίου, λιωμένα τούβλα μαγνησίας-χρωμίου, λιωμένα, λεπτά αλεσμένα και στη συνέχεια συγκολλημένα τούβλα μαγνησίας-χρωμίου. Χρησιμοποιούνται ευρέως σε φούρνους ανοιχτής εστίας, επαγωγικούς φούρνους κ.λπ. Μεταλλουργικός μετατροπέας και επένδυση περιστροφικών κλιβάνων τσιμεντοβιομηχανίας κ.λπ.
Στη βιομηχανία χυτηρίου, το μετάλλευμα χρωμίου δεν αλληλεπιδρά με άλλα στοιχεία του τηγμένου χάλυβα κατά τη διαδικασία έκχυσης, έχει χαμηλό συντελεστή θερμικής διαστολής, είναι ανθεκτικό στη διείσδυση μετάλλων και έχει καλύτερη απόδοση ψύξης από το ζιρκόνιο. Το μεταλλεύμα χρωμίου για χυτήρια έχει αυστηρές απαιτήσεις σχετικά με τη χημική σύνθεση και την κατανομή μεγέθους σωματιδίων.
Στη χημική βιομηχανία, η πιο άμεση χρήση του χρωμίου είναι η παραγωγή διαλύματος διχρωμικού νατρίου (Na2Cr2O7·H2O) και στη συνέχεια η παρασκευή άλλων ενώσεων χρωμίου για χρήση σε βιομηχανίες όπως χρωστικές, υφάσματα, ηλεκτρολυτική επιμετάλλωση και κατασκευή δέρματος, καθώς και καταλυτών .
Η λεπτοαλεσμένη σκόνη μεταλλεύματος χρωμίου είναι ένας φυσικός χρωστικός παράγοντας για την παραγωγή γυαλιού, κεραμικών και εφυαλωμένων πλακιδίων. Όταν το διχρωμικό νάτριο χρησιμοποιείται για την καταστροφή του δέρματος, η πρωτεΐνη (κολλαγόνο) και οι υδατάνθρακες στο αρχικό δέρμα αντιδρούν με χημικές ουσίες για να σχηματίσουν ένα σταθερό σύμπλεγμα, το οποίο γίνεται η βάση των δερμάτινων προϊόντων. Στην κλωστοϋφαντουργία, το διχρωμικό νάτριο χρησιμοποιείται ως μυρωδάτο στη βαφή υφασμάτων, το οποίο μπορεί να συνδέσει αποτελεσματικά μόρια βαφής σε οργανικές ενώσεις. Μπορεί επίσης να χρησιμοποιηθεί ως οξειδωτικό στην παρασκευή βαφών και ενδιάμεσων προϊόντων.
Ορυκτό χρώμιο
Υπάρχουν περισσότερα από 50 είδη ορυκτών που περιέχουν χρώμιο που έχουν ανακαλυφθεί στη φύση, αλλά τα περισσότερα από αυτά έχουν χαμηλή περιεκτικότητα σε χρώμιο και διάσπαρτη κατανομή, η οποία έχει χαμηλή βιομηχανική αξία χρήσης. Αυτά τα ορυκτά που περιέχουν χρώμιο ανήκουν σε οξείδια, χρωμικά και πυριτικά άλατα, εκτός από μερικά υδροξείδια, ιωδικά, νιτρίδια και σουλφίδια. Μεταξύ αυτών, το νιτρίδιο του χρωμίου και τα ορυκτά θειούχου χρωμίου βρίσκονται μόνο σε μετεωρίτες.
Ως ορυκτό είδος στην υποοικογένεια του μεταλλεύματος χρωμίου, ο χρωμίτης είναι το μόνο σημαντικό βιομηχανικό ορυκτό του χρωμίου. Ο θεωρητικός χημικός τύπος είναι (MgFe)Cr2O4, στον οποίο η περιεκτικότητα σε Cr2O3 αντιστοιχεί στο 68%, και στο FeO στο 32%. Στη χημική του σύσταση, το τρισθενές κατιόν είναι κυρίως Cr3+ και συχνά υπάρχουν ισομορφικές υποκαταστάσεις Al3+, Fe3+ και Mg2+, Fe2+. Στον πραγματικό παραγόμενο χρωμίτη, μέρος του Fe2+ αντικαθίσταται συχνά από Mg2+ και το Cr3+ αντικαθίσταται από Al3+ και Fe3+ σε διάφορους βαθμούς. Ο πλήρης βαθμός ισομορφικής υποκατάστασης μεταξύ των διαφόρων συστατικών του χρωμίτη δεν είναι συνεπής. Τα κατιόντα συντονισμού τεσσάρων τάξεων είναι κυρίως μαγνήσιο και σίδηρος, και η πλήρης ισομορφική υποκατάσταση μεταξύ μαγνησίου-σιδήρου. Σύμφωνα με τη μέθοδο των τεσσάρων διαιρέσεων, ο χρωμίτης μπορεί να χωριστεί σε τέσσερις υποομάδες: χρωμίτης μαγνησίου, χρωμίτης σιδήρου-μαγνήσιου, χρωμίτης μαφικού σιδήρου και χρωμίτης σιδήρου. Επιπλέον, ο χρωμίτης περιέχει συχνά μια μικρή ποσότητα μαγγανίου, Ένα ομοιογενές μείγμα τιτανίου, βαναδίου και ψευδαργύρου. Η δομή του χρωμίτη είναι κανονικού τύπου σπινελίου.
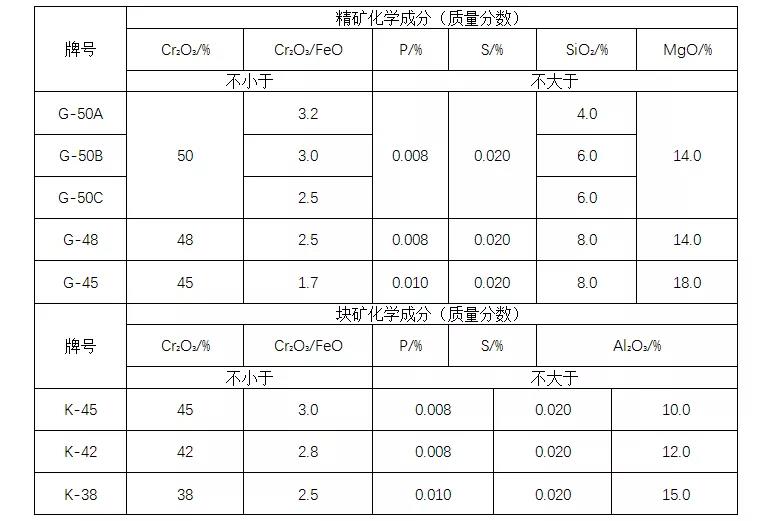
4. Πρότυπο ποιότητας του συμπυκνώματος χρωμίου
Σύμφωνα με διαφορετικές μεθόδους επεξεργασίας (ανοργανοποίηση και φυσικό μετάλλευμα), το μετάλλευμα χρωμίου για τη μεταλλουργία χωρίζεται σε δύο τύπους: το συμπύκνωμα (G) και το χονδρόκοκκο μετάλλευμα (Κ). Δείτε τον παρακάτω πίνακα.
Απαιτήσεις ποιότητας για μετάλλευμα χρωμίτη για τη μεταλλουργία
Τεχνολογία εμπλουτισμού μεταλλεύματος χρωμίου
1) Επανεκλογή
Επί του παρόντος, ο βαρυτικός διαχωρισμός κατέχει σημαντική θέση στον εμπλουτισμό του μεταλλεύματος χρωμίου. Η μέθοδος διαχωρισμού με βαρύτητα, η οποία χρησιμοποιεί χαλαρή στρωματοποίηση στο υδατικό μέσο ως βασική συμπεριφορά, εξακολουθεί να είναι η κύρια μέθοδος για τον εμπλουτισμό του μεταλλεύματος χρωμίου παγκοσμίως. Ο εξοπλισμός διαχωρισμού βαρύτητας είναι ένας σπειροειδής αγωγός και ένας φυγοκεντρικός συμπυκνωτής και το εύρος μεγέθους σωματιδίων επεξεργασίας είναι σχετικά ευρύ. Γενικά, η διαφορά πυκνότητας μεταξύ ορυκτών χρωμίου και ορυκτών γάγγας είναι μεγαλύτερη από 0,8 g/cm3 και ο διαχωρισμός βαρύτητας οποιουδήποτε μεγέθους σωματιδίου μεγαλύτερο από 100um μπορεί να είναι ικανοποιητικός. το αποτέλεσμα του. Το μετάλλευμα χονδροειδών σβώλων (100 ~ 0,5 mm) ταξινομείται ή προεπιλέγεται με εμπλουτισμό βαρέως μέσου, που είναι μια πολύ οικονομική μέθοδος εμπλουτισμού.
2) Μαγνητικός διαχωρισμός
Ο μαγνητικός διαχωρισμός είναι μια μέθοδος εμπλουτισμού που πραγματοποιεί διαχωρισμό ορυκτών σε ένα μη ομοιόμορφο μαγνητικό πεδίο με βάση τη μαγνητική διαφορά των ορυκτών στο μετάλλευμα. Ο χρωμίτης έχει ασθενείς μαγνητικές ιδιότητες και μπορεί να διαχωριστεί με κατακόρυφους δακτυλίους μαγνητικούς διαχωριστές υψηλής κλίσης, μαγνητικούς διαχωριστές υγρής πλάκας και άλλο εξοπλισμό. Οι ειδικοί συντελεστές μαγνητικής επιδεκτικότητας των ορυκτών χρωμίου που παράγονται σε διάφορες περιοχές παραγωγής μεταλλευμάτων χρωμίου στον κόσμο δεν διαφέρουν πολύ και είναι παρόμοιοι με τους ειδικούς συντελεστές μαγνητικής επιδεκτικότητας του βολφραμίτη και του βολφραμίτη που παράγονται σε διάφορες περιοχές.
Υπάρχουν δύο περιπτώσεις κατά τη χρήση του μαγνητικού διαχωρισμού για τη λήψη υψηλής ποιότητας συμπυκνώματος χρωμίου: η μία είναι η αφαίρεση των ισχυρών μαγνητικών ορυκτών (κυρίως ο μαγνητίτης) στο μετάλλευμα κάτω από ένα ασθενές μαγνητικό πεδίο για να αυξηθεί η αναλογία σιδηροχρωμίου και η άλλη είναι η χρήση ισχυρό μαγνητικό πεδίο. Διαχωρισμός ορυκτών γάγγας και ανάκτηση μεταλλευμάτων χρωμίου (ασθενώς μαγνητικά ορυκτά).
3) Ηλεκτρική επιλογή
Ο ηλεκτρικός διαχωρισμός είναι μια μέθοδος διαχωρισμού μεταλλεύματος χρωμίου και ορυκτών πυριτικών γατών χρησιμοποιώντας τις ηλεκτρικές ιδιότητες των ορυκτών, όπως οι διαφορές στην αγωγιμότητα και η διηλεκτρική σταθερά.
4) Επίπλευση
Κατά τη διαδικασία διαχωρισμού με βαρύτητα, το λεπτόκοκκο μετάλλευμα χρωμίτη (-100um) απορρίπτεται συχνά ως απορρίμματα, αλλά ο χρωμίτης αυτού του μεγέθους εξακολουθεί να έχει υψηλή αξία χρήσης, επομένως η μέθοδος επίπλευσης μπορεί να χρησιμοποιηθεί για χαμηλής ποιότητας λεπτόκοκκο μετάλλευμα χρωμίτη ανακτάται. Επίπλευση μεταλλεύματος χρωμίου με 20% ~ 40% Cr2O3 σε απορρίμματα και ορυκτά σερπεντίνης, ολιβίνης, ρουτιλίου και ανθρακικού ασβεστίου μαγνησίου ως ορυκτά γάγγας. Το μετάλλευμα αλέθεται λεπτή στα 200μm, υαλοπίνακας νερού, φωσφορικά, μεταφωσφορικά, φθοριοπυριτικά κ.λπ. χρησιμοποιούνται για τη διασπορά και την αναστολή της ιλύος και ως συλλέκτης χρησιμοποιείται ακόρεστο λιπαρό οξύ. Η διασπορά και η καταστολή της λάσπης λάσπης είναι πολύ σημαντική για τη διαδικασία επίπλευσης. Τα ιόντα μετάλλων όπως ο σίδηρος και ο μόλυβδος μπορούν να ενεργοποιήσουν τον χρωμίτη. Όταν η τιμή pH του πολτού είναι κάτω από 6, ο χρωμίτης δύσκολα θα επιπλέει. Εν ολίγοις, η κατανάλωση αντιδραστηρίου επίπλευσης είναι μεγάλη, η ποιότητα του συμπυκνώματος είναι ασταθής και ο ρυθμός ανάκτησης είναι χαμηλός. Τα Ca2+ και Mg2+ που διαλύονται από ορυκτά γάγγας μειώνουν την επιλεκτικότητα της διαδικασίας επίπλευσης.
5) Χημικός εμπλουτισμός
Η χημική μέθοδος είναι η άμεση επεξεργασία ορισμένων μεταλλευμάτων χρωμίτη που δεν μπορούν να διαχωριστούν με φυσική μέθοδο ή το κόστος της φυσικής μεθόδου είναι σχετικά υψηλό. Ο λόγος Cr/Fe του συμπυκνώματος που παράγεται με χημική μέθοδο είναι υψηλότερος από αυτόν της συνηθισμένης φυσικής μεθόδου. Οι χημικές μέθοδοι περιλαμβάνουν: επιλεκτική έκπλυση, αναγωγή οξείδωσης, διαχωρισμό τήξης, έκπλυση θειικού οξέος και χρωμικού οξέος, αναγωγή και έκπλυση θειικού οξέος κ.λπ. Ο συνδυασμός φυσικοχημικών μεθόδων και η άμεση επεξεργασία του μεταλλεύματος χρωμίου με χημικές μεθόδους είναι ένας από τους κύριους τάσεις στον εμπλουτισμό χρωμίτη σήμερα. Οι χημικές μέθοδοι μπορούν να εξαγάγουν απευθείας χρώμιο από το μετάλλευμα και να παράγουν καρβίδιο του χρωμίου και οξείδιο του χρωμίου.
Ώρα δημοσίευσης: Απρ-30-2021